AutorIn
Heinz Stutzenberger, so erschienen im Alpha1-Journal 2/2025.
Der Alpha-1-Antitrypsin-Mangel, kurz AATM, des Genotyps Pi*Z ist auf dem besten Wege, eine Art Prototyp für neue gentechnische Behandlungsmethoden zu werden, die auf der Beeinflussung der DNA (= Desoxyribonukleinsäure) bzw. RNA (= Ribonukleinsäure) basieren. Grund dafür ist die Tatsache, dass diese Form des AATM durch ein einziges falsches (mutiertes) Basenpaar an einer genau definierten Stelle der Erbsubstanz verursacht wird, und damit leichter zu behandeln sein wird als andere vererbbare Veranlagungen oder Krankheiten, die durch eine Mehrzahl von Mutationen verursacht werden.
Bei dieser Ausgangssituation ist es naheliegend, dass sich Alphas ein tieferes Verständnis der Zusammenhänge verschaffen, und diesem Zweck diente ein Webinar, das die Alpha-1 Europe Alliance, also die Dachorganisation der nationalen europäischen Alpha-1-Vereine, für ihre Mitgliedervertreter veranstaltet hat. Die Präsentation wurde gehalten von Marion Bouchekareilh, die am Bordeaux Forschungsinstitut für Translationale Onkologie zum Thema AATM forscht, und die als Gast für Frankreich an den monatlichen Mitgliederversammlungen der Alpha-1 Europe Alliance teilnimmt. Ihre Ausführungen sind im Folgenden zusammengefasst:
Die Erbinformation des Menschen, die Aufbau, Funktion und Reparatur des Körpers steuert, ist in der DNA gespeichert. Diese befindet sich im Zellkern und besteht aus ca. sechs Milliarden Basenpaaren, die in Form einer Doppelwendel angeordnet sind. Nur vier verschiedene Basen finden dabei Verwendung, bezeichnet mit den Buchstaben A, T, C und G. Neben anderen Informationen sind in der DNA auch die Vorschriften kodiert, nach denen in den Leberzellen (Hepatozyten) Proteine hergestellt werden, z. B. auch Alpha-1-Antitrypsin. Beim AATM mit dem Genotyp PI*ZZ steht nun an zwei definierten Stellen der DNA je ein falsches Basenpaar, DNA- und RNA-Eingriffe zur Behandlung des Alpha-1- Antitrypsin-Mangels 45 in dessen Folge das danach gebildete Protein etwas anders als das normale AAT-Molekül ausgeformt bzw. falsch gefaltet ist. Infolge dieser Fehlfaltung neigt es zum Verklumpen und kann die Leberzellen nicht mehr verlassen: Der Alpha-1-Antitrypsin-Mangel entsteht.
Bei der Bildung von Proteinen können die Zellen allerdings nicht direkt auf die DNA als Vorlage zurückgreifen, die im Zellkern eingeschlossen ist. Stattdessen wird von der DNA eine Art Kopie erstellt, als RNA bezeichnet, die aus dem Zellkern ausgeschleust wird und die Produktion der Proteine steuert. Fehler in der DNA finden sich dann natürlich auch in der RNA wieder. Für die Bildung eines speziellen Proteins wird allerdings nur die Kopie eines bestimmten Abschnittes der DNA benötigt. Die Kopie eines solchen Abschnittes, den es für jedes im Körper gebildete Protein gibt, wird mRNA genannt, also Messenger-RNA, auf Deutsch Botenstoff- RNA.
Die neuartigen Medikamente setzen nun an den unterschiedlichen Stellen der Proteinbildung an:
• entweder durch Veränderung/Korrektur der DNA
• oder durch Veränderung/Korrektur der mRNA
• oder durch Ausschaltung der mRNA (und damit der Vermeidung der spezifischen Proteinbildung)
Je nach dem Ziel des Eingriffes kommen unterschiedliche Techniken zum Einsatz.
Zur Veränderung der DNA wird das CRISPR-Cas9-Verfahren eingesetzt, also die sogenannte Genschere. Dabei wird ein größerer Abschnitt der DNA in den Leberzellen, der die fehlerhafte Information enthält, ausgeschnitten und durch einen korrigierten Abschnitt ersetzt, sodass nach der Behandlung in den betroffenen Zellen normales AAT gebildet wird. Die so erzielte Veränderung der DNA in den Leberzellen wird bei der permanenten Zellerneuerung weitergegeben, sodass es sich bei dieser Behandlung im Idealfall um eine einmalige Gabe des Wirkstoffes handelt, deren Auswirkung dann lebenslang erhalten bleibt. Mit diesem Vorteil einher geht dann aber auch eines der Risiken dieser Behandlung: Bei der Anwendung der Genschere können unbeabsichtigt auch benachbarte Basenpaare verändert werden, was zu ungewollten Nebenwirkungen führen könnte, die dann aber auch lebenslang erhalten bleiben. Mit der Entwicklung einer entsprechenden Therapie befasst sich die Firma Beam Therapeutics; Intellia hat die Entwicklung für AATM Ende 2024 eingestellt (und der klinische Versuch für ein Medikament einer anderen Krankheit musste wegen eines ungeklärten Todesfalles unterbrochen werden (Stand 11.2025).
mRNA wird permanent gebildet und auch wieder abgebaut. Eingriffe auf RNA-Ebene haben deshalb nur einen vorübergehenden Einfluss, ein die mRNA modifizierendes Medikament muss deshalb regelmäßig verabreicht werden. Mit der sog. ADAR-Technik kann gezielt ein einziges Basenpaar auf der mRNA repariert werden, wodurch das Risiko unerwünschter Nebenwirkungen schon einmal deutlich reduziert wird. Sollten diese dennoch auftreten, ist damit zu rechnen, dass sie abnehmen, in dem Maße, in dem die modifizierte mRNA im Körper abgebaut wird, und Nebenwirkungen damit typischerweise nach einigen Wochen wieder abgeklungen sind. Entsprechende Medikamente werden zurzeit entwickelt von den Firmen WAVE, KORRO, PrimeMedicine, ADARx und AIRNA.
Die Z-Variante von Alpha-1 Antitrypsin
Die Z-Mutation ist eine kleine „Veränderung“ in der DNA – ein bisschen wie ein Typo-Fehler in einem Text.
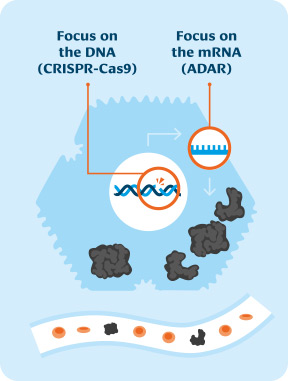
Therapeutische Strategie
Wie können wir Schädigungen, die durch die Z-Variante verursacht werden, vorbeugen? Wir reparieren die Z-Variante.
Auch wenn die beiden oben beschriebenen neuartigen Behandlungsmethoden bereits eingetretene Lungenschädigungen nicht werden heilen können, so ist ihr Ziel, die Leber so zu beeinflussen, dass eine ausreichende Menge funktionalen AATs gebildet und zumindest die schützende Konzentration von M-AAT erreicht wird (die sog. protektive Schwelle), wie z. B. bei einem typischen PI*MZ Merkmalsträger. Dadurch sollte die Lunge vor weiteren Schäden geschützt sein und die Leber sich von Einlagerungen polymerisierten Z-AATs erholen können. Voraussetzung dafür ist, dass das eingesetzte Medikament einen ausreichend hohen Anteil an Leberzellen erreicht, und in diesem Aspekt werden sich die Ansätze der verschiedenen Entwickler unterscheiden.
Die dritte Möglichkeit eines Eingriffs ist die siRNA, die small interfering RNA, auf Deutsch kleine eingreifende RNA. Dabei handelt es sich um kurze RNA-Stränge, die dem Körper zugeführt werden, sich dann an die Ziel-mRNA binden und diese auflösen, bevor sie zur Bildung des ihr zugeordneten Proteins wirksam wird. Durch diese Behandlung wird also die Bildung jeglichen AATs verhindert, sodass sich eine durch verklumptes Z-AAT beeinträchtigte Leber wieder erholen kann. Ein entsprechendes Medikament wird von Takeda entwickelt, aufbauend auf Vorarbeiten von Arrowhead.
All diesen Wirkstoffen ist gemeinsam, dass sie aus sehr großen Molekülen bestehen, die biotechnologisch hergestellt werden. Diese lassen sich nicht einfach wie chemisch hergestellte Wirkstoffe in Tabletten pressen oder Kapseln füllen. Auch wäre eine orale Gabe nicht zielführend, da die Wirkstoffe im Verdauungstrakt abgebaut würden und ihr Ziel, nämlich die Leberzellen, gar nicht erreichen würden. Stattdessen werden die Wirkstoffe in komplexe „Vehikel“ verpackt, die so aufgebaut sind, dass sie nach einer Gabe unter die Haut (subkutan) oder ins Blut (intravenös) direkt von den Leberzellen aufgenommen werden und dort ihre Wirkung entfalten können.
Die Vortragende hatte übrigens auch eine sehr bildhafte Darstellung dieser doch recht komplexen Zusammenhänge angeboten, die das Verständnis eventuell erleichtert: Dabei kann man die DNA als eine Art Kochbuch begreifen, in dem die Rezepte für Aufbau und Funktion des Körpers abgelegt sind. RNA ist dann zu verstehen als eine Kopie desselben. Sowohl die Vorlage als auch die Kopie enthalten Kapitel zur Erzeugung von Proteinen. mRNA ist dann eine Kopie einer Seite mit dem Rezept zur Herstellung eines bestimmten Proteins. In diesem Bild ist eine Mutation dann ein Fehler im Rezeptbuch bzw. dessen Kopie, und im Falle des AAT ist ein einziger Buchstabe an einer genau bekannten Stelle falsch. Bei einem Eingriff in die DNA wird nun aus dem Rezeptbuch das ganze, den Fehler enthaltende, Kapitel herausgeschnitten und durch ein neues ersetzt, das natürlich keine neuen Fehler enthalten sollte. Im Falle des RNA-Eingriffs wird auf der Kopie einer Seite des Rezeptbuches nur ein einziger Buchstabe ausradiert und neu beschrieben, wobei die Kopie insgesamt aber rasch verblasst. siRNA führt dazu, dass die kopierte Seite verblasst, bevor sie gelesen werden kann.
Erfreulicherweise befinden sich also eine Fülle von DNA bzw. RNA-basierten Medikamenten in der Entwicklung bzw. in den verschiedenen Phasen der klinischen Erprobung. Hier kommen jetzt wir, die Menschen mit AATM, ins Spiel, da für die klinische Erprobung Probanden benötigt werden. Allerdings rekrutieren einige der Programme keine Probanden in Deutschland, da hier die Substitutionstherapie weitverbreitet ist, deren Anwendung die Teilnahme an manchen Programmen verhindert. Oft sind aber die Einschlusskriterien der Studien etwas weiter gefasst, sodass auch Programme in Deutschland durchgeführt werden.
Interessiert an einer Medikamentenstudie?
Wenn Sie an der Teilnahme an einer Medikamentenstudie interessiert sind, schauen Sie auf unsere Internetseite unter der Rubrik „Wissenswertes“ auf die Seite „Forschung und Studien“ oder klicken Sie hier.
Bilder wurden mit freundlicher Genehmigung von Marion Bouchekareilh bereitgestellt.

